2024年12月4日,來自國加州大學(xué)的Lawrence Fong團(tuán)隊,在國際知名期刊Nature(IF:50.5)發(fā)表了題為“ Evolution of myeloid-mediated immunotherapy resistance in prostate cancer”的研究性論文。研究人員利用單細(xì)胞RNA測序技術(shù),通過對處于不同疾病階段的前列腺癌患者腫瘤樣本活檢的分析發(fā)現(xiàn),SPP1高表達(dá)的腫瘤相關(guān)巨噬細(xì)胞 (SPP1hi-TAM) 亞群隨疾病進(jìn)展而富集。并通過腺苷信號通路抑制CD8+ T細(xì)胞活性,最終導(dǎo)致免疫治療的耐藥性。研究進(jìn)一步表明,阻斷腺苷A2A受體(A2AR)不僅可以有效降低SPP1hi-TAMs的免疫抑制作用,還顯著提高了免疫檢查點抑制劑PD1等的療效。強(qiáng)調(diào)了SPP1hi-TAM作為治療靶點和預(yù)測治療效果的潛在生物標(biāo)志物的重要性。

前列腺癌是最常見的男性惡性腫瘤,雄激素剝奪療法(ADT) 最初可引起臨床反應(yīng),但大多數(shù)晚期前列腺癌患者最終進(jìn)展為轉(zhuǎn)移性去勢抵抗性前列腺癌(mCRPC) 并死于這種疾病。近年來,針對CTLA-4、PD-1和PD-L1的免疫檢查點抑制劑 (ICIs) 已被批準(zhǔn)治療多種癌癥,但mCRPC患者對此療法通常不盡人意。腫瘤微環(huán)境 (TME) 是促進(jìn)多種惡性腫瘤免疫治療耐藥中扮演重要校色,大量證據(jù)表明髓系細(xì)胞如腫瘤相關(guān)巨噬細(xì)胞(TAMs) 和髓系抑制性細(xì)胞(MDSCs) 可通過多種機(jī)制介導(dǎo)前列腺癌的免疫抑制,這些細(xì)胞的豐度在ADT后顯著增加,這意味著它們在mCRPC中具有驅(qū)動免疫治療耐藥的作用。然而,這些髓系細(xì)胞種類多樣、功能復(fù)雜,使得針對它們的治療策略面臨巨大挑戰(zhàn)。例如,盡管CSF1R(集落刺激因子1受體)阻斷劑曾被寄予厚望,但在臨床試驗中未能顯著改善患者的預(yù)后。如何深入理解髓系細(xì)胞在前列腺癌免疫抑制中的具體機(jī)制,成為破解治療耐藥難題的關(guān)鍵。
在癌癥研究中,髓系細(xì)胞一直是一把“雙刃劍”。它們在健康狀態(tài)下負(fù)責(zé)維持免疫平衡,但在癌癥環(huán)境中卻常被腫瘤“招募”并“改造”,成為促進(jìn)腫瘤生長和免疫抑制的幫兇。特別是在前列腺癌的腫瘤微環(huán)境中,髓系細(xì)胞不僅數(shù)量眾多,功能也復(fù)雜多樣,包括腫瘤相關(guān)巨噬細(xì)胞(tumor-associated macrophages, TAMs)、髓系抑制細(xì)胞(myeloid-derived suppressor cells, MDSCs)和樹突狀細(xì)胞(dendritic cells, DCs)等。研究發(fā)現(xiàn),這些髓系細(xì)胞通過釋放多種免疫抑制因子(如IL-10、TGF-β)和代謝產(chǎn)物(如腺苷),削弱了T細(xì)胞和自然殺傷細(xì)胞(NK細(xì)胞)的抗腫瘤活性。然而,髓系細(xì)胞并不是單一的群體,而是一個異質(zhì)性極高的“大家族”。例如,TAMs就分為M1型(促炎性、抗腫瘤性)和M2型(抗炎性、促腫瘤性),它們的比例和功能會隨著腫瘤的進(jìn)展而動態(tài)變化。這種復(fù)雜性使得針對髓系細(xì)胞的治療策略面臨巨大挑戰(zhàn)。
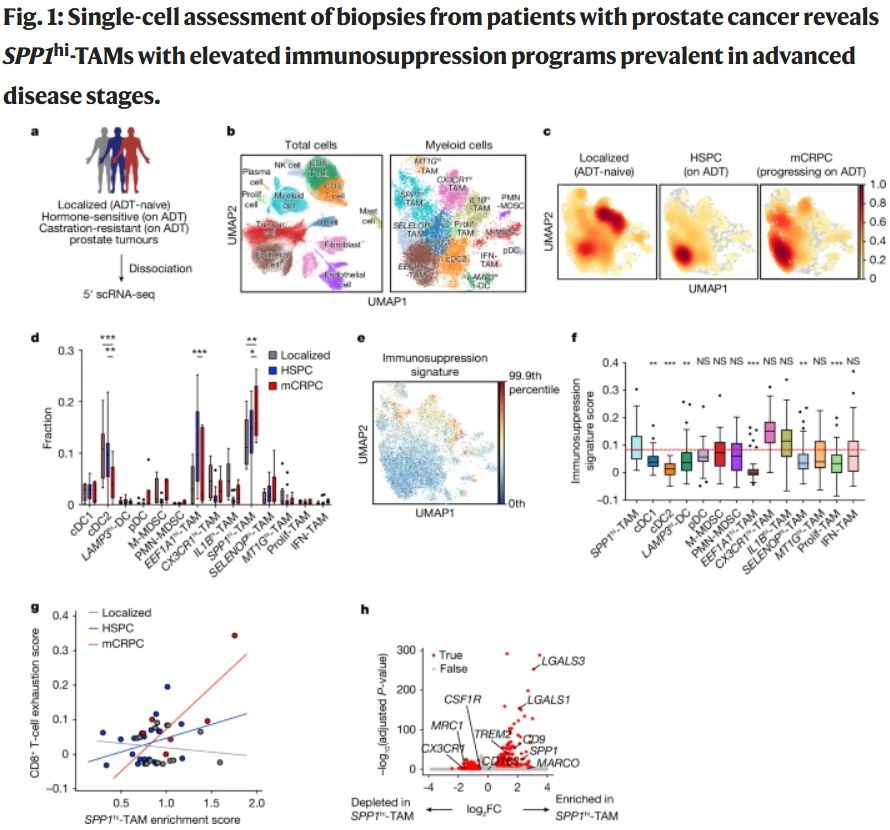
為了確定在疾病進(jìn)展過程中起作用的免疫抑制性細(xì)胞,他們對不同階段 (ADT初治局部非轉(zhuǎn)移性、ADT敏感轉(zhuǎn)移性、mCRPC) 的前列腺癌患者的腫瘤活檢樣本進(jìn)行scRNA-seq,髓系細(xì)胞被細(xì)分為14種亞群,包括8種巨噬細(xì)胞亞群、2種髓系抑制細(xì)胞亞群和3種樹突狀細(xì)胞亞群等。其中發(fā)現(xiàn)一組以SPP1高表達(dá)、免疫抑制分子程序上調(diào)、集落刺激因子-1受體 (CSF1R) 轉(zhuǎn)錄水平顯著降低為特征的SPP1高度表達(dá)巨噬細(xì)胞亞群 (SPP1hi-TAM) 隨疾病進(jìn)展顯著增加,此外,體外培養(yǎng)結(jié)果顯示這群細(xì)胞以密度依賴的方式顯著抑制T細(xì)胞增殖,且導(dǎo)致IFN-γ+TNF-α+ CD8+ T細(xì)胞的頻率顯著降低,提示SPP1hi-TAM可能是mCRPC免疫治療耐藥的潛在驅(qū)動因素。
作者進(jìn)一步在小鼠模型中驗證人類研究結(jié)果,并探索Spp1hi-TAMs對免疫治療抵抗的作用。使用MyC-CaP小鼠前列腺癌模型進(jìn)行單細(xì)胞RNA測序,并通過流式細(xì)胞術(shù)驗證結(jié)果。在小鼠前列腺癌中也識別出與人類SPP1hi-TAMs相似的Spp1hi-TAMs,其表達(dá)Spp1、Cd9和Lgals3轉(zhuǎn)錄本水平升高,而Csf1r、Mrc1、Cx3cr1和Cd163表達(dá)降低。Spp1hi-TAMs對CSF1R阻斷治療表現(xiàn)出抵抗性,其數(shù)量在治療后未顯著減少。Spp1hi-TAMs在小鼠前列腺癌中表現(xiàn)出較高的免疫抑制基因表達(dá)特征。

為了探究SPP1hi-TAM促進(jìn)免疫治療耐藥性的機(jī)制,該團(tuán)隊進(jìn)一步分析了人類和小鼠前列腺癌的scRNA-seq數(shù)據(jù)集,發(fā)現(xiàn)缺氧途徑顯著激活,已知缺氧可通過上調(diào)CD39和CD73促進(jìn)腫瘤細(xì)胞外腺苷的積累,與腺苷受體A2ARs和A2BRs結(jié)合后可通過胞內(nèi)cAMP啟動下游免疫抑制信號傳導(dǎo),降低T細(xì)胞和NK細(xì)胞抗腫瘤活性。為了直接測試SPP1hi-TAM是否是通過腺苷抑制T細(xì)胞活性,他們將其與CD8+ T細(xì)胞在A2ARs的小分子抑制劑ciforadenant以及CD73的阻斷抗體存在下共培養(yǎng),這兩種處理均會導(dǎo)致SPP1hi-TAM介導(dǎo)的T細(xì)胞抑制顯著降低,表明了腺苷信號通路在SPP1hi-TAMs介導(dǎo)的免疫抑制中起關(guān)鍵作用。基于此發(fā)現(xiàn),他們隨后檢查了用ciforadenant治療攜帶CRPC的小鼠是否可以改變體內(nèi)的抗腫瘤反應(yīng),發(fā)現(xiàn)SPP1hi-TAM數(shù)量和CRPC生長都顯著降低,將該抑制劑與抗PD-1抗體聯(lián)合使用能增強(qiáng)CD8+T細(xì)胞的瘤內(nèi)浸潤并進(jìn)一步抑制腫瘤生長。研究人員進(jìn)行一項1期臨床試驗,將mCRPC患者隨機(jī)分為兩組,一組接受ciforadenant單獨治療,另一組接受ciforadenant與atezolizumab聯(lián)合治療。聯(lián)合治療組中有25%的患者前列腺特異性抗原(PSA)水平下降30%以上,并且一些患者出現(xiàn)腫瘤縮小。基于SPP1hi-TAMs的豐度可能作為治療效果的預(yù)測生物標(biāo)志物,但需要更大樣本量的研究來進(jìn)一步驗證。
總之,PP1hi-TAMs可以作為一種重要的生物標(biāo)志物,幫助預(yù)測免疫治療的效果。在臨床試驗中,研究人員發(fā)現(xiàn)患者腫瘤組織中SPP1hi-TAMs的豐度與聯(lián)合治療的療效顯著相關(guān)。通過檢測SPP1hi-TAMs的水平,醫(yī)生或許能夠篩選出更有可能受益于A2AR抑制劑與免疫檢查點抑制劑聯(lián)合治療的患者群體,從而實現(xiàn)個性化治療。另外,SPP1hi-TAMs本身也是一個極具潛力的治療靶點。SPP1hi-TAMs通過腺苷信號通路抑制抗腫瘤免疫反應(yīng),同時還能通過其他促炎性因子(如IL-1β)進(jìn)一步惡化腫瘤微環(huán)境。未來的研究可以進(jìn)一步探索更多抑制SPP1hi-TAMs功能或減少其數(shù)量的方法,例如針對腺苷信號通路和炎癥因子的雙靶點治療策略,從而從源頭上瓦解免疫抑制。
荷蘭Liposoma的單核巨噬細(xì)胞清除劑氯膦酸二鈉脂質(zhì)體Clodronate Liposomes,氯膦酸鹽脂質(zhì)體,廣泛用于動物體內(nèi)單核巨噬細(xì)胞的清除。研究成果頻頻登刊Cell,Nature和Science。國內(nèi)研究人員如需訂購,可以隨時聯(lián)系。技術(shù)支持可以聯(lián)系大中華獨家代理商靶點科技(Target Technology),專業(yè)技術(shù)團(tuán)隊給您單核巨噬細(xì)胞清除提供整套解決方案。
原始文獻(xiàn)
Lyu, A., Fan, Z., Clark, M. et al. Evolution of myeloid-mediated immunotherapy resistance in prostate cancer. Nature (2024). https://doi.org/10.1038/s41586-024-08290-3
關(guān)聯(lián)研究:CXCL9:SPP1巨噬細(xì)胞極性確定來控制人類癌癥的細(xì)胞程序網(wǎng)絡(luò)
2023年8月4日,瑞士日內(nèi)瓦大學(xué)領(lǐng)導(dǎo)的國際研究團(tuán)隊在Science(IF=56.9)發(fā)表了研究論文:CXCL9:SPP1 macrophage polarity identifies a network of cellular programs that control human cancers。由 CXCL9 和 SPP1 這兩個基因的表達(dá)所定義的巨噬細(xì)胞極性的變化是腫瘤微環(huán)境的一個簡單而關(guān)鍵的特征。CXCL9:SPP1的比例可以描述癌癥中抗腫瘤免疫細(xì)胞的豐度、每種腫瘤浸潤細(xì)胞類型的基因表達(dá)程序、決定腫瘤控制或進(jìn)展的通訊網(wǎng)絡(luò)的調(diào)控以及對免疫療法的反應(yīng)。

獨家代理
中國大陸地區(qū)
生產(chǎn)廠家
歐洲荷蘭王國
獨家代理
香港臺灣澳門
Copyright ? 2004-2023 靶點科技(北京)有限公司. 版權(quán)所有. 京ICP備18027329號-1