結核分枝桿菌(Mycobacterium tuberculosis),俗稱結核桿菌,導致一種被稱作肺結核的破壞性疾病。它每年殺死140萬人并且導致1000萬例新增的病例。當肺部的巨噬細胞吞噬入侵的結核分枝桿菌時,它們原本應當會破壞這種病原菌,但是這種病原菌進化出逃避這種破壞并繼續生長的能力。結核分枝桿菌(Mtb)通過抑制細胞凋亡和促進壞死來殺死受感染的巨噬細胞。結核壞死性毒素(TNT)是分泌的煙酰胺腺嘌呤二核苷酸(NAD +)糖水解酶,其在受感染的巨噬細胞中誘導壞死。
3年前,美國阿拉巴馬大學伯明翰分校的Michael Niederweis博士及其團隊有史以來發現了結核分枝桿菌的首個毒素。與幾乎所有其他的病原菌產生的毒素不同的是,這種毒素并不導致疾病或死亡。他們將這種毒素稱為結核壞死性毒素(tuberculosis necrotizing toxin, TNT),并證實TNT屬于一類新的之前未被識別的存在于600多種細菌和真菌物種中的毒素。他們還發現TNT酶促水解NAD+---所有活細胞中的一種至關重要的輔酶,而且巨噬細胞中的NAD +缺乏在一定程度上會導致巨噬細胞經歷壞死性細胞死亡,從而釋放出結核分枝桿菌來感染更多的細胞。這種壞死性細胞死亡使得巨噬細胞偏離它們破壞被吞噬的細菌的正常途徑---在巨噬細胞內對被吞噬的細菌進行溶酶體降解,從而觸發巨噬細胞經歷程序性細胞死亡(或者說細胞凋亡)。
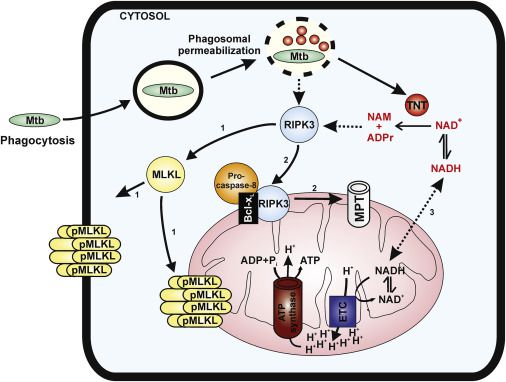
在一項新的研究中,Niederweis團隊展示了TNT如何幫助結核分枝桿菌贏得與人體免疫細胞之間的戰斗,從而控制被感染的巨噬細胞的命運,這是決定著這種感染結果的關鍵性戰斗。相關研究結果發表在2018年7月10日的Cell Reports期刊上,論文標題為“NAD+ Depletion Triggers Macrophage Necroptosis, a Cell Death Pathway Exploited by Mycobacterium tuberculosis”。
巨噬細胞的基因編碼的蛋白組成一種導致程序性壞死(也被稱作壞死性凋亡)的經典通路,這個通路能夠被免疫系統激活。Niederweis團隊發現,由TNT水解導致的NAD+損耗激活這個通路中的兩個關鍵的調節物:RIPK3和MLKL,從而繞過這個通路中的兩個上游組分。與此同時,作為細胞能量工廠的線粒體發生去極化,并且為細胞提供大部分化學能的ATP分子的合成受到損害。
令人吃驚的是,當Niederweis團隊通過抑制NAD+補救途徑中的一種酶來降低未被感染的巨噬細胞中的NAD +水平時,通過RIPK3和MLKL通路發生的壞死也被激活。這表明僅是NAD +損耗也足以誘導壞死性(necroptosis),即便當TNT和結核分枝桿菌不存在時,也是如此。
這一發現提出了一個問題:給被結核分枝桿菌感染的巨噬細胞補充NAD+能夠減輕由TNT引起的細胞毒性嗎?Niederweis團隊發現,往被感染的巨噬細胞的體外培養物中加入煙酰胺(NAD+前體分子)可將巨噬細胞的活力增加三倍。類似地,在被感染的巨噬細胞中加入保護線粒體的化合物---通過增加線粒體數量從而增加線粒體呼吸率或者通過阻止線粒體通透性形成--也會增加線粒體膜電位和細胞活力三到四倍。再者,所有的這些處理方法都會限制結核分枝桿菌在巨噬細胞內的生長。
Niederweis說,“我們發現NAD+耗損觸發程序性細胞死亡來殺死被結核分枝桿菌感染的巨噬細胞,這揭示出開發針對肺結核的宿主靶向療法的策略。”
這可能包括使用被美國FDA批準的藥物來降低壞死性凋亡,為患者補充NAD+,或者使用促進線粒體功能的試劑,以及將這些方法與用于治療肺結核的抗菌藥物組合使用。這些針對患者的策略也可能適用于治療導致NAD +損耗的其他細菌和真菌病原體感染。
原始出處:David Pajuelo, Norberto Gonzalez-Juarbe, Uday Tak et al. NAD+ Depletion Triggers Macrophage Necroptosis, a Cell Death Pathway Exploited by Mycobacterium tuberculosis. Cell Reports, 10 July 2018, 24(2):429–440, doi:10.1016/j.celrep.2018.06.042.

獨家代理
中國大陸地區
生產廠家
歐洲荷蘭王國
獨家代理
香港臺灣澳門
Copyright ? 2004-2023 靶點科技(北京)有限公司. 版權所有. 京ICP備18027329號-1